Absolute asymmetrische Synthese
Wissenschaftliche Mitarbeiter und Mitarbeiterinnen: Michael Haak; Thorsten Marquardt; Michael Plagmann; Jens Schmeyers; Prof. Dr. Z. Rappoport, Jerusalem, Israel; Prof. Dr. J. Scheffer, Vancouver, Kanada; Prof. Dr. M. Demuth, Mülheim; Prof. Dr. F. Toda, Marsuyama, Japan
Projektbeschreibung: Bei der "absoluten asymmetrischen Synthese" wird im Gegensatz zur "symmetrischen Synthese" ohne chirale Hilfsmittel Chiralität erzeugt. Geeignete achirale Molekule können in chiralen Raumgruppen kristallisieren. Zufällig (oder gezielter durch Impfung) erhält man große Mengen von Kristallen einer einzigen Chiralität. Diese Chiralität wird bei Festkörperreaktionen weitgehend erhalten, wenn asymmetrische Moleküle entstehen.
Stand: fortlaufend
Kooperation mit: University of Jerusalem, Israel; UC, Vancouver, Kanada; MPI Kohleforschung, Mülheim; Ehime University, Matsuyama, Japan
Ausgewählte Veröffentlichungen:
Kaupp, Gerd; Haak, Michael: Absolute asymmetric synthesis by irradiation of chiral crystals. - In: Angewandte Chemie. International Edition in English. - 32 (1993), S. 694 - 695
Kaupp, Gerd: Resolution of racemates by distillation with inclusion compounds. - In: Angewandte Chemie. International Edition in English. - 33 (1994), S. 728 - 729
Kaupp, Gerd; Marquardt, Thorsten: Absolute asymmetric synthesis solely under the influence of a static homoneneous magnetic field?. - In: Angewandte Chemie. International Edition in English. - 33 (1994), S.1459 -146.
Kaupp, Gerd; Schmeyers, Jens; Toda, Fumio; Takumi, Hideaki; Koshima, Hideko: Mechanism of solid-solid resolutions of ([plus minus]) pantolactone. - In: Journal of physical organic chemistry. - 9 (1996), S. 795 - 800
AFM
Wissenschaftliche Mitarbeiter und Mitarbeiterinnen: Dr. Andreas Herrmann; Axel Kuse; Jürgen Boy; Prof. Dr. F. Toda, Matsuyama, Japan
Projektbeschreibung: Die Mechanismen der organischen Festkörperreaktionen, die außer den sehr seltenen topotaktischen Photoreaktionen, mit den bisherigen Theorien nicht verstanden werden, wurden aufgeklärt, um sie für abfallfreie Produktionstechniken von morgen nutzen zu können. Dies erforderte den erstmaligen Einsatz der neuen Technik Kraftmikroskopie (AFM).
Laufzeit: 8/94 - 8l95
Fremdfinanzierung: DFG
Kooperation mit: Ehime University, Matsuyama, Japan
Ausgewählte Veröffentlichungen:
Kaupp, Gerd; Schmeyers, Jens: Gas/solid reactions of aliphatic amines with thiohydantoines: atomic force microscopy and new mechanisms. - In: Angewandte Chemie <Weinheim>. -104 (1993), S.1656 -1658
Kaupp, Gerd: AFM on chemically reacting crystals. - In: Molecular and crystal liquid crystals science and technology. Section A, Molecular crystals and liquid crystals. - 242 (1994), S.153 -169
Kaupp, Gerd; Plagmann, Michael: Atomic force microscopy and solid state photolyses: phase rebuilding. - In: Joumal of photochemistry and photobiology. A, Chemistry. - 80 (1994), S. 399 - 407
Kaupp, Gerd: Nanostructures of submicrostructures from gas/solid reactions as probed by atomic force microscopy. - In: Joumal of vaccum science & technology. B, Microelectronics and nanometer structure processing, measurement and phenomena. -12 ( 1994), S.1952 -1956
Kaupp, Gerd; Haak, Michael; Toda, Fumio: Atomic force microscopy and solid state rearragement of benzopinacol. - In: Joumal of physical organic chemistry. - 8 (1995), S. 545- 551
Atmosphäreentgiffung
Wissenschaftliche Mitarbeiter und Mitarbeiterinnen: Dr. Uwe Pogodda; Karin Dartsch; Jens Schmeyers
Projektbeschreibung: Organische Lösungsmitteldämpfe sind in vielfacher Hinsicht atmosphärenschädlich und müssen möglichst am Ort ihrer Entstehung aus der Atmosphäre entfernt werden. Ein attraktiver weg ist die quantitative Reaktion der Spurengase mit geeigneten Kristallen unter Bildung von Wertprodukten oder regenerierbaren Clathraten. Laufzeit: 8/90 - 3/93
Fremdfinanzierung: BM B F -
Ausgewählte Veröffentlichungen:
Kaupp, Gerd: Minderung organischer Luftschadstoffemissionen mittels Gas/Festkörper-Reaktionen. - In: DLR Umweltschutztechnik. - (1993), S. 453
Kaupp, Gerd; Pogodda, Uwe; Bartsch, Karin; Schmeyers, Jens; Ulrich, A.; Reents, E.; Janiel, M.: Minderung organischer Lutschadstoffemissionen mittels Gas-/FestkörperReaktionen: Teilvorhaben 1: wissenschaftlich-technische Begleitung. - In: BMFT Forschungsbericht. -1993. - (...; 01 VQ9027). - S.1- 47
Kaupp, Gerd: Reactions in supercritical carbon dioxide. - In: Angewandte Chemie. International Edition in English. - 33 (1994), S.1452 -1455
Kaupp, Gerd; Pogodda, Uwe; Schmeyers, Jens: Gas/solid-reactions with acetone. - In: Chemische Berichte. -127 (1994), S. 2249 - 2261
Kaupp, Gerd; Jaskulska, E.; Sauer, G.; Michl, G.: Neue Produkte der Ringerweiterungen von 17-Hydroxy-20-ketosteroiden. - In: Journal für praktische Chemie, Chemiker- Zeitung. - 336 (1994), S. 686 - 689
Kraftmikroskopie bei Festkörperreaktionen
Wissenschaftliche Mitarbeiter und Mitarbeiterinnen: Dr. Jens Schmeyers; Dr. Andreas Herrmann; Michael Haak; Thorsten Marquardt; Heinz Knöringer; Jürgen Boy; Axel Kuse; Prof. Dr. F. Toda, Matsuyama, Japan
Projektbeschreibung: Die Kraftmikroskopie zeigt; daß Festkörperreaktionen freistufig ablaufen. Dies läßt sich mit den Kristallpackungen korrelieren, wodurch Voraussagen für weitere quantitativ und abfallfrei verlaufende Gas/Festkörper und Festkörper/Festkörper Reaktionen ohne flüssige Phase möglich werden.
Stand: fortlaufend
Fremdfinanzierung: DFG
Kooperation mit: Ehime University, Matsuyama, Japan
Ausgewählte Veröffentlichungen:
Kaupp, Gerd; Schmeyers, Jens; Haak, Michael; Marquardt, Thorsten; Herrmann, Andreas: AFM in organic solid state reactions. - ln: Molecular crystals and liquid crystals sciences and technology. Section A, Molecular crystals and liquid crystals. - 276 (1996), S. 315 - 337
Kaupp, Gerd; Schmeyers, Jens: Gas/solid reactions with nitrogen dioxide. - In: Journal of organic chemistry. - 60 (1995), S. 5494 - 5503
Kaupp, Gerd: Cyclobutane synthesis in the, solid state. - In: CRC handbook of organic photochemistry and photobiology / ed. William M. Horspool... -1. [print.). - Boca Raton, Fla. (U.a.), 1995. - S. 50 - 56
Kaupp, Gerd; Schmeyers, Jens; Haak. Michael; Herrmann, Andreas: Kraftmikroskopie zur Aufklärung abfallfreier Festkörpersynthesen. - In: Labo-Trend. - 95 (1995), S. 57 - 63
Kaupp, Gerd: Atomic force microscopy on photoreactive organic solids: nanostructures. In: Molecular and crystals liquid crystals science and technology. Section A, Molecular crystals and liquid crystals. - 252 (1994), S. 259 - 268
Laserphotochemie / Festkörperphotochemie, Strahleninduzierte Prozesse
Wissenschaftliche Mitarbeiter und Mitarbeiterinnen: Andreas Vogel; Michael Haak; Olaf Sauerland -
Projektbeschreibung: Mit Lasern lassen sich im Megawattbereich biphotoniale Photoreaktionen erreichen, die mit normalen Lichtintensitäten nicht gelingen. Erfolgreich waren nicht nur Umlagerungen, Zerfall und Additionen niedermolekularer organischer Verbindungen mit Hetreocyclen sondern auch die maßgeschneiderte Herstellung von Oligonmeren mit scharfen Molekulargewichtsverteilungen.
Stand: fortlaufend
Fremdfinanzierung: BMBF
Ausgewählte Veröffentlichungen:
Kaupp, Gerd: (4 + 4)-Cycloadditionen in der Totalsynthese natülrlich vorkommender Achtringverbindungen. - In: Angewandte Chemie <Weinheim>. -104 (1993), S. 783 - 785
Kaupp, Gerd: (2 + 2)-cyclobutane-synthesis (liquid phase). - In: CRC handbook of organic photochemistry and photobiology / ed. William M. Horspool... -1. (print.). - Boca Raton, Fla. (u.a.), 1995. - S. 29 - 49.
Kaupp, Gerd: 6,7-diphenyl-2,3-dihydro-1,4-dioxocine. - In: Photochemical key steps in organic synthesis / J. Mattay... (eds.). - Weinheim (u.a.),1994. - S. 224 - 225
Kaupp, Gerd: 2-(1,2-diphenylethenyl) benzothiazole. - In: Photochemical key steps in organic synthesis / J. Mattay... (eds.). - Weinheim (u.a.),1994. - S.130 -133
SNOM-Messungen
Wissenschaftliche Mitarbeiter und Mitarbeiterinnen: Dr. Andreas Herrmann; Michael Haak
Projektbeschreibung: Es wird die für organische Oberflächen, die regelmäßig sehr rauh sind, verwendbare SNOM-Technik ermittelt. Die derzeit favorisierten Geräte mit metallbedampften Meßspitzen sind ungeeignet, da sich letztere in 5-10 mm Abstand auf > 100°C aufheizen. Ohne thermische Effekte sind nur metallbedampfungsfreie Spitzen in DME SNOM nach Courjon Technik. -
Laufzeit: 10/95 - 9/96
Fremdfinanzierung: DFG
Ausgewählte Veröffentlichungen:
Kaupp, Gerd: AFM and STM in photochemistry including photon tunneling. - In: Advances in photochemistry. -19 (1995), S.119 -177
Kaupp, Gerd: Supermicroscopy in supramolecular chemistry: AFM, SNOM, and SXM. - In: Comprehensive supramolecular chemistry. - Oxford. - 8 (1996), S. 381- 423
Kaupp, Gerd; Haak, Michael: EIZ-Photoisomerisierung in Kristallen. - In: Angewandte Chemie <Weinheim>. -108 (1996), S. 2948 - 2951
Tetraazaazulene / Tetrazocin
Wissenschaftliche Mitarbeiter und Mitarbeiterinnen: Prof. Dr. U. Pietsch, Potsdam; Priv. Doz. J. Staupe; Sabine Bembenek; Sven Krüger; Michael Haak
Projektbeschreibung: Die cytostatische Wirkung von Coformicin, die HIV-1-Wirksamkeit von TIBO und andere Anwendungen legen nahe, unser neues Konzept der cyclisierenden Aminomethylenierung noch weiter auszubauen. Der Baustein Methylenchlorid ermöglicht Reaktionen, die mit Formaldehyd nicht gelingen und auch völlig neue Hexaazapolycyclen selektiv erhalten lassen.
Laufzeit: 7/90 -11/94
Fremdfinanzierung: DFG
Kooperation mit: Universität Potsdam; Humboldt Universität Berlin
Ausgewählte Veröffentlichungen:
Sailer, Kaus: Substitutions- und Cyclisierungsreaktionen von 2-Chlormethylbenzimidazolen mit Aminen und Dichlormethan. -1993. - Oldenburg, Univ., Diss.,1993
Kaupp, Gerd; Sailer, Klaus: Hexaazapolycyclen durch selektive Multimethylenierung mit Dichlormethan und Base oder mit Utropin. - In: Journal für praktische Chemie, Chemiker-Zeitung. - 338 ( 1996), 6, S. 47 - 50
Kaupp, Gerd; Denisenko, Sergej N.: 13C NMR spectra of tricyclic diaziridines and their data-base forecasts. - In: Magnetic resonance in chemistry. - 30 (1992), S. G37 - 639
Geue, T.; Stumpe, J.; Möbius, G.; Pietsch, U.; Schuster, A.; Ringsdorf, H.; Kaupp, Gerd: Photoinduced optical anisotropy and microphase-separation processes of LangmuirBlodgett multilayer assemblies containing amphotropic azocopolymer. - In: Journal of informatic recording materials - Joumal für Signalaufzeichnungsmaterialien. - 21 ( 1994), S. 645 - 650
Geue, T.; Stumpé, J.; Pietsch, U.; Haak, Michael; Kaupp, Gerd: Photochemically induced changes of optical anisotropy and surface of LB-multilayers built up by an amphiphilic and liquid crystalline copolymer containing azobenzene moieties. - In: Molecular crystals and liquid crystals sciences and technology. Section A, Molecular crystals and liquid crystals. - 262 (1995), S.157 -166
Erforschung von Systemlösungen für transparente Verschleiß-schutzschichten auf Kunststoffen - Teilvorhaben: organische Schichten und organische Haftvermittlungsschichten mit kovalenter Anbindung
Wissenschaftliche Mitarbeiter und Mitarbeiterinnen: Dr. Jens Schneyers; Dr. Uwe Pogodda; Michael Haak; Thorsten Marquardt; Michael Plagmann
Projektbeschreibung: Die Anwendung der Kraftmikroskopie (AFM) auf organische Oberflächen einschließlich polymerer mit und ohne Lichteinwirkung wurden untersucht, um Grundlagen zu schaffen für die direkte Messung des Erfolgs monomolekularer kovalent chemischer Beschichtung von CR39, PC, PU und PMMA.
Laufzeit: 9/93 - 8/96
Fremdfinanzierung: BMBF ülber VDI Technologiezentrum
Kooperation mit: Leica GmbH, Wetzlar; Rupp u. Hubrach KG, Bamberg; Jenoptik GmbH, Jena: Leybold AG, Hanau;
Ausgewählte Veröffentlichungen:
Kaupp, Gerd; Schmeyers, Jens: Organische Schichten und organische Haftvermittlungsschichten mit konvalenter Anbindung, Oberflächen- und Schichttechnologien. - In: Oberflächen- und Schichttechnologien / VDI-Technologiezentrum. - Düsseldorf,1995.S. 76 - 82
Kaupp, Gerd; Schmeyers, Jens; Pogodda, Uwe; Haak, Michael; Marquardt, Thórsten; Plagmann, Michaef: AFM for the imaging of large and steep submicroscopic features, artifacts and scraping with asymmetric cantilever tips. - In: Thin solid films. - 264 (1995), 5.205-211
Kaupp, Gerd: Kraftmikroskopie: Ergebnisse bei Photodimerisierungen. - In: GIT : Labor Fachzeitschrift. - 37 (1993), S. 284 - 294
Kaupp; Gerd: Kraftmikroskopie: Ergebnisse bei Photodimerisierungen ; II. Teil. - In: GIT : Labor-Fachzertschrift. - 37 (1993), S. 581- 586
Kaupp, Gerd: Atomic force microscopy in the photochemistry of chalcones. - In: Journal of microscopy. -174 (1994), S.15 - 22
Mítglieder der Arbeitsgruppe
Dipl.Chem. Cornelia Schröder geb. Haase (nach Promotion ausgeschieden)
Dipl.Chem. Torsten Braams (nach Promotion ausgeschieden)
Dipl.Chem. Holger Kelm (nach Promotion ausgeschieden)
Dipl.Chem. Harald Kopatz (nach Promotion ausgeschieden)
Dipl.Chem. Manfred Dromowitz (nach Promotion ausgeschieden)
Dipl.Chem. Thorsten Kern (nach Promotion ausgeschieden)
Dipl.Chem. Angelika Wernicke
Dipl.Chem. Arne Lützen
Dipl.Chem. Andrea Gansz
Dipl.Chem. Jan de Boer
Dipl. Chem. Robert Saul
Dipl.Chem. Rainer Bruns
Dipl. Chem. Michael Stöver
Cand. chem. Heike Klimscha (nach Diplomierung ausgeschieden)
Cand. chem. Peter von Hagel (nach Diplomierung ausgeschieden)
Cand. chem. Thomas Kowalik (nach Diplomierung ausgeschieden)
Ing. Herbert Komander, TA
Rosemarie Raphael, Sekretariat
Diplomarbeiten
Im Berichtszeitraum wurden folgende Diplomarbeiten erfolgreich abgeschlossen:
Peter von Hagel Untersuchungen zur Konformation von Pyranosen mit einem annelierten Fünfring
Heike Klimscha Reaktionen ausgewählter Keto- Disaccharide mit Kaliumcyanat und Kaliumthiocyanat
Thomas Kowalik Isopropylidenierung von Nitroalditolen unter kinetischer Kontrolle
Robert Saul Die Umsetzung von 1,3-Diaminoaceton-hydrochlorid mit Kaliumthiocyanat, Kaliumcyanat und Cyanamid
Rainer Bruns Versuche zur Darstellung von Glykonperoxiden
Michael Stöver Unkonventionelle Synthesen in der Kohlenhydratchemie
Doktorarbeiten
Im Berichtszeitraum wurden folgende Promotionsvorhaben erfolgreich abgeschlossen:
Cornelia Schröder Kettenverlängerung von Kohlenhydraten mit Hilfe von Samariumdiíodid
Torsten Braams Nitroalditole und Nitroenalditole: Neue geschützte Derivate
Holger Kelm Alkylierungen,Desoxygenierungen und
Didesoxyeliminierungen an Sedoheptulosan (2,7-Anhydro-ß-D-altro-heptulopyranose) im Hinblick auf die Entwicklung neuer Zugänge zu enantiomerenreinen Semiochemikalien
Harald Kopatz Neue Verfahren zur Herstellung von Edukten für C-Glykosid-Synthesen über 1-Azide von 2,5-Anhydroalditolen
Manfred Dromowicz Oxidation von 2,6-Anhydrodes-oxynitroalditolen mit Wasserstoffperoxid zu 2,6-Anhydroaldonsäuren und deren Überführung in Ester und Amide
Thorsten Kern Die Reaktion ausgewählter Mono- und Disaccharide mit Cyanat, Thiocyanatund Cyanamid
Forschung
Nutzung, Synthese und Konformationsanalyse von Kohlenhydraten ("Zuckern")
Kohlenhydrate sind die Schlüsselsubstanzen allen Lebens auf der Erde. Sie stellen den Hauptteil organischer Substanz in der aktiven Biosphäre und sind daher die wichtigsten sich durch ständig ablaufende Photosynthese regenerierenden Rohstoffe für die Energienutzung und die chemische Synthese. Darüber hinaus zeichnen sie sich vor allen anderen Naturstoffen durch Polyfunktionalität bei komplexer Stereochemie aus. Sie stellen daher eine besondere Herausforderung an die Fähigkeiten des Organischen Chemikers. Im hiesigen Arbeitskreis werden wichtige und aktuelle Aspekte der Chemie dieser Verbindungsklasse bearbeitet, wobei die Untersuchungen im Bereich der Synthese vor allem darauf abzielen, möglichst direkte und daher kostengünstige Wege zu Wertprodukten unter Vermeidung toxischer Reagentien und umweltbelastender Verfahren zu finden und zu entwickeln.
Die insgesamt bearbeiteten Fragestellungen können wie folgt systematisiert werden:
a) "Biomassenutzung" (Erforschung "Nachwachsender Rohstoffe"): Methoden zur gezielten Veredelung von "Massenkohlenhydraten", wie Glucose, Lactose, Sorbit, Xylit u.ä. .
b) Synthesen: Synthesen von Anhydrozuckern, von Nitrozuckern und deren Anhydriden, von Glycosylcyaniden, von cyclischen Carbamaten von Glycosylaminen, von Flüssigkristallen auf der Basis Kohlenhydrate/Fette, von langkettigen Zuckeralkoholen; Kettenverlängerung von Zuckern, Radikalreaktionen an Polyhydroxyverbindungen, Entwicklung neuer Chiralika sowie grundsätzlich die Fortentwicklung von Methoden für stereoselektive Synthesen.
c) Struktur-, insbesondere Konformationsanalyse der genannten Substrate mittels hochauflösender NMR-Spektroskopie, Röntgenstrukturanalyse, Massenspektrometrie und semiempirischer Modellierungen.
C XVIII International Carbohydrate Symposium (Mailand, Italien, 21.-26.7.1996):
P. Köll, J. Kopf, S. Pohl, W. Saak, A. Gansz, P. v. Hagel und J. de Boer: "The UsuaI/Unusual Conformations of Pyranoses Anullated to a Five-membered Ring in 1,2-Position".
M. Petrusová, D.-P. Pham-Huu, J. N. BeMiller, P. Köll und L. Petrus: " Full Acetals of C-(ß-D-Glucopyranosyl)nitromethanes and of a 1,2-Dideoxy-1-Nitroalk-1-enitol derived from common Hexoses".
A. Gansz und P. Köll: " Synthesis of four octitols from 2.3:4,5-di-O-isopropylidenealdehydo-D-arabinose".
P. Köll und A. Lützen : "Acetal protected Glyco-oxazolidin-2-ones as Versatile Chiral Auxiliaries".
P. Köll und A. Wernicke: "The Total Synthesis of (+)-Goniofufurone and its 7-Epimer from D-Glucose".
Wissenschaftliche Kooperationen mit Partnern außerhalb der Universität Oldenburg
Prof. Dr. Jürgen Kopf, Institut für Anorganische und Angewandte Chemie der Universität Hamburg (D) (Konformationsanalyse: Röntgendiffraktometrie).
Prof. Dr. István Pintér und Dr. Jószef Kovács, Zentralforschungsinstitut für Chemie der Ungarìschen Akademie der Wissenschaften, Budapest (H) (Zuckercarbamate).
Prof. Dr. J. F. Verchère und Dr. Stella Chapelle, Fachbereich Chemie der Universität Rouen (F) (Molybdän- und Wolframkomplexe von Zuckeralkoholen).
Dr. Ladislav Petrus und Dr. Maria Petrusová, Institut für Chemie der Slovakischen Akademie der Wissenschaften, Bratislava (SR) (Nitrozucker).
Prof. Dr. John S. McKinley-McKee, Institut für Biochemie der Universität Oslo (N) (Substratspezífität von Alkoholdehydrogenasen).
Fremdfinanzierung: DAAD, Fonds der Chemischen Industrie, Stipendienfonds der Chemischen Industrie, DFG.
Die genannten Fragestellungen wurden im Rahmen von sechs Diplomarbeiten (abgeschlossen, s.o.) und dreizehn Doktorarbeiten (davon 6 abgeschlossen, s.o.) sowie in Zusammenarbeit mit mehreren auswärtigen Forschergruppen (s.u.) untersucht. Von den erzielten Ergebnissen wurde bisher leider nur ein Teil endgültig veröffentlicht (s.u.). Allerdings wurden die wesentlichsten Ergebnisse auf zwei internationalen und einem nationalem Kongreß vorgestellt (s.u.).
Verzeichnis der Publikationen im Berichtszeitraum
J. Kovács, I. Pintér und P. Köll; "Direct transformation of D-idose and D-altrose with potassium cyanate into cycfic carbamates of derived glycosyamines", Carbohydr Res.1995,272, 255-262.
S. Chapelle, J.-P. Sauvage, P. Köll und J.-F. Verchère: 183W NMR studies of Tungstate Complexes of Carbohydrates.3. Species formed with all-threo Aldìtols acting as tridentate, tetradentate, or pentadentate Ligands", Inorg. Chem. 1995, 34, 918-923.
P. Köll und A. Lützen: "Resolution of Racemic Carboxylic and Sulfonic Acids via DXylose Derived New Cyclic Carbamate Reagents (Oxazolidin-2-ones)", Tetrahedron: Asymmetry 1995, 6, 43-46.
P. Köll und A. Lützen: "D-Xylose Derived Oxazolidin-2-ones as Chiral Auxiliaries in Stereoselective Alkylations", Tetrahedron:Asymmetry 1996, 7, 637-640.
Kongreßbeiträge
A VIII European Carbohydrate Symposium (Sevilla, Spanien, 2.-7.7.1995): P. Köll, J. Kopf, S. Pohl, W. Saak, A. Gansz und P. v. Hagel: "The UsuaIlUnusual Conformations of Pyranoses Anullated to a Five-membered Ring in 1,2-Position". P. Köfl, I. Pintér und T. Kern: " Preparation and resolution of racemic 4,9-Diaza-2,7- dioxospiro(4.4)nonane-3,8-dithione derived from dihydroxyacetone".
P. Köll, J. Kovács und A. Wernicke: "Synthesis of 3,6- and 3,7-Anhydro-lactones by Reaction of Meldrums Acid with Aldoses".
P. Köll und A. L`ützen: "New Oxazolidin-2-one Reagents derived from D- Xylose as Chiral Auxiliaries.
J. Kovács, I. Pintér, T. Kern und P.Köll: "Simple Synthesis of 1,2-Fused Oxazoiidin-2- one Derivatives of Disaccharides".
B 25. GDCh-Hauptversammlung (Münster,10.-16.9.1995):
A. Wernicke und P. Köll: "Darstellung von 3,6- und 3,7-Anhydro-1,4-lactonen durch Umsetzung von Meldrumsäure mit Aldosen".
A. Gansz und P. Köll: "Synthese von vier Octitolen aus 2,3:4,5-Di-O-ísopropyliden- aldehydo-D-arabinose.
Mitglieder der Arbeitsgruppe
Burghard Stigge (TA)
Markus Tiepold (Diplomand)
Peter Vagedes (Diplomand)
Andreas Willecke (Diplomand)
Anja Braams (Doktorandin)
Stefan Freimund (Doktorand)
Susanne Hüsken (Doktorandin)
Jörg Richter (Diplomand)
Kooperationen
Prof. Dr. Friedrich Giffhorn, Institut für Mikrobiologie, Universität Saarbrücken
Prof. Dr. Bernd Meyer, Institut für Organische Chemie, Universität Hamburg
Prof. Dr. Thomas Peters, Medizinische Universität zu Lübeck
Prof. Dr. Uri Zehavi, Hebrew University of Jerusalem, Israel
Einladungen zu Vorträgen im Berichtszeitraum
im Inland:
an den Universitäten in Braunschweig, Lübeck, Ulm, Köln, Karlsruhe und Heidelberg,
sowie den Firmen Hoechst Marion Roussel (Pharm. Div. of Hoechst AG), Marburg und Dr. Karl Thomae GmbH, Biberach.
im Ausland:
an den Universitäten in Graz (ÖS), Vancouver (Kanada) und Washington (USA) sowie dem Scripps Institute, La Jolla (USA).
Fremdfinanzierung
Finanzielle Förderung durch die DFG, das BMBF, den Fonds der Chemischen Industrie, die Volkswagenstiftung.
Sach- oder Finanzmittel außerdem von der Hoechst AG und Boehringer Mannheim.
Forschung
Das Forschungsgebiet der Gruppe umfaßt die Bereiche: Enzymkatalysierte organische Synthesen und Biosynthesen mit Kohlenhydraten, Struktur/Funktionsbeziehungen in diesen Systemen und Konformationsanalyse sowie mit Hilfe NMR-Spektroskopischer Methoden und theoretischen Molekülberechnungen.
Enzymatische Oxidationen an Kohlenhydraten
Projektleitung: PD Dr. S. Köpper.
Beteiligter Wissenschaftler: Stefan Freimund.
Kooperation mit Prof. Dr. Friedrich Giffhorn und Axel Huwig am Institut für Mikrobiologie der Universität Saarbrücken.
Oxidoreduktasen (Enzyme) aus Weißfäulepilzen können Glucose zu einer chemisch interessanten Keto-ulose oxidieren. Im Hinblick auf die Verwendung nachwachsender Rohstoffe wird die Möglichkeit untersucht, mit diesem Enzym andere Kohlenhydrat-Substrate zu oxidieren. Mögliche Substrate und deren enzymatische Produkte werden chemisch charakterisiert und bezüglich ihrer Verwendung als Vorstufen für technisch interessante Folgeprodukte untersucht.
Die als Oxidationsprodukte anfallenden 2- oder 3-Keto-Aldosen bilden in Lösung komplexe Gleichgewichtsgemische von fünf bis 15 verschiedenen isomeren Formen. Die Zusammensetzung dieser Gemische wird mit Hilfe der NMR-Spektoskopie aufgeklärt.
Enzymatische Oligosaccharidsynthese
Projektleitung: PD Dr. S. Köpper
Beteiligte Wissenschaftler: Peter Vagedes.
Kooperation mit Prof. Uri Zehavi, Hebrew University of Jersualem, Israel.
Biologisch aktive Oligosaccharide, die sich z.B. in Glycoshingoplipidstrukturen finden lassen, und Modifikationen, deren biologische Aktivität zu testen ist, werden durch Reaktionen auf polymeren Trägern synthetisiert. Die Syntheseprodukte lassen sich durch Bestrahlung mit sichtbarem Licht leicht vom polymeren Träger abspalten und die Glycosylierung erfolgt mit Glycosyltransferasen oder durch Transglycosylierungsreaktionen mit Hydrolasen oder Phosphatasen.
Das Projekt wurde im November 1996 begonnen.
Modifikation von Substraten für Glycosyltransferasen
Projektleitung: PD Dr. S. Köpper
Beteiligte Wissenschaftler: Anja Braams, Susanne Hüsken, Markus Tiepold, Peter Vagedes.
Eine Herleitung von Struktur/Wirkungsbeziehungen zwischen Glycosyltransferasen und ihren Donoren, den Nucleotidzuckern, ist Ziel dieses Projektes. Durch die Kenntnis dieser Wirkungsbeziehungen sollte es einerseits möglich sein, einen genaueren Einblick in die Reaktionsmechanismen dieser essentiellen Enzyme (im menschlichen Organismus) zu gewinnen und gegebenenfalls Inhibitoren solcher Reaktionen für medizinische und biochemische Anwendungen zu synthetisieren. Andererseits können synthetisierbare Donoren konzipiert werden, die die präparative Nutzung der Enzyme wesentlich verbessern.
Im Projekt werden synthetische Modifikationen der Donormoleküle erzeugt und diese auf ihre biologische Aktivtität mit der Glycosyltransferase hin untersucht.
Konformationsanalyse von Nucleosiden und Nucleotidzuckern
Projektleitung: PD Dr. S. Köpper
Beteiligte Wissenschaftler: Jörg Richter, Peter Vagedes und Andreas Willecke.
Kooperation mit Prof. Dr. Bernd Meyer, Universität Hamburg
Die dreidimensionale Struktur einer chemischen Verbindung und ihre Flexibilität ist das entscheidende Kriterium für ihre Reaktivität und biologische Wirkung. In Anlehnung an das Projekt ‘Modifikation von Substraten für Glycosyltransferasen’ werden Nucleoside, Nucleotide, Nucleotidzucker und ihre modifizierten Varianten konformationsanalytisch untersucht. Experimentell werden hierbei NMR-Verfahren wie die Messung von NOE-Verstärkungen an isolierten Molekülen und Transfer-NOEs an Komplexen eingesetzt, sowie theoretische Molekülberechnungen mit Molekular-Dynamik Verfahren und Kraftfeldrechnungen vorgenommen.
Diplomarbeiten im Berichtszeitraum
Markus Tiepold Synthese basenmodifizierter Uridindiphospho-Galactoside.
Jörg Richter Konformationsuntersuchungen an UDP-Glucose und UDP-Galactose mit Hilfe NMR-spektroskopischer Methoden.
Thomas Haselhorst Konformationsanalyse einer verzweigten Pentasaccharidsequenz in N-Glycoproteinen (teilweise an der Medizinischen Universität zu Lübeck)
Dissertationen im Berichtszeitraum
Anja Braams Synthese und Konformationsbetrachtungen modifizierter Nucleotidzucker als Donorsubstrate für den enzymatischen Glycosyltransfer.
Stefan Freimund Enzymatische Oxidationen mit Pyranose-2-Oxidase: Herstellung und Charakterisierung von Keto-Aldosen.
Veröffentlichungen
S. Köpper and B. Meyer, Liebigs Ann. Chem., 1996, 1131-1137. Restricted Flexibility of the Glycosidic Linkage in a(1à3) linked L-Digitoxosides as determined by NMR Spectroscopy and MMC Calculations.
S. Köpper, GIT Fachz. Lab. 6, 624-631 (1996). Bestimmung der Konformation und Flexibilität von Desoxy-Oligosacchariden: die Lösungskonformation des Antibiotikums Kijanimicin.
M. Hatam, J. Martens, and S. Köpper, Heterocycles, 43, 675 - 683 (1996). The Diastereoselective Synthesis of Oxacephams from 1,3-2H-Oxazines.
M. Hatam, S. Köpper, and J. Martens, Heterocycles, 43, 1653-1663 (1996). Synthesis of Homohydantoin-Thiazolidine Bicyclic Compounds.
S. Freimund, A. Huwig, F. Giffhorn, and S. Köpper, J. Carbohydr. Chem., 15, 115 -120 (1996). Convenient Chemo-Enzymatic Synthesis of Tagatose.
S. Köpper, Kombinatorik, Enzyme und Leitstrukturen, Nachr. Chem. Tech. 10, 984-987 (1996).
S. Freimund, F. Giffhorn, A. Huwig, and S. Köpper, eingereicht. Rare Keto-Aldoses from Enzymic oxidation: Substrates and Oxidation Products of Pyranose-2-Oxidase.
S. Köpper and S. Freimund, J. Carbohydr. Chem. eingereicht, The composition of hexose 2- and 3-uloses in solution as determined by NMR spectroscopy.
S. Köpper and S. Freimund, Carbohydr. Res., eingereicht. Dimeric Structures and Elimination Products of 1,5-Anhydro-D-fructose.
Präsentationen auf Konferenzen
S. Köpper, S. Freimund, A. Huwig und F. Giffhorn, Irseer Naturstofftage, Irsee 1996: Herstellung wertvoller Ketozucker durch Enzymatische Oxidation.
S. Köpper, A. Huwig, F. Giffhorn, and S. Freimund, I st. Lausanne Conference on Bioorganic Chemistry, Lausanne, März 1996: Rare Keto Sugars from Enzymic Oxidation.
S. Köpper, A. Braams und S. Hüsken, Chemiedozentagung, Hannover 1996: Modifizierte Donorsubstrate für Galactosyltransferase.
S. Köpper, A. Huwig, F. Giffhorn, und S. Freimund, XVIII International Carbohydrate Symposium, Mailand, Juli 1996: Rare Keto Sugars from Enzymic Oxidation.
A. Braams, S. Hüsken, A. Willecke, und S. Köpper, 1. East European Carbohydrate Workshop, Güstrow, März 1996: Synthesis and Conformational Analysis of Modified Sugar Nucleotides and Nucleosides.
Mitglieder der Arbeitsgruppe (1995/96)
Doktoranden
Dipl.- Chem. Willi Behnen (Promotion 1996)
Dipl.- Chem. Christine Dauelsberg (Promotion 1996)
Dipl.- Chem. Mostafa Hatam (Promotion 1996)
Dipl.- Chem. Jens Manikowski
Dipl.- Chem. Thomas Mehler (Promotion 1995)
Dipl.- Chem. Jörg Wilken
Dipl.- Chem. Viola Peper
Dipl.- Chem. Wilhelm Trentmann
Dipl.- Chem. Iris Reiners
Dipl.- Chem. Hajo Thümler
Apotheker Bernd Roder
Dipl.- Chem. Harald Gröger
Dipl.- Chem. Jürgen Eilers
Dipl.- Chem. Michael Kossenjans
Dipl.- Chem. Helmut Pennemann
Dipl.- Chem. Imre Schlemminger
Diplomanden
Silke Erny
Marc Gehrke
Marc Redmann
Jan de Buer
Wolfgang Maison
Michael Wohlberg
Wertstoffsynthese aus Abfallstoffen der chemischen Industrie
Projektleitung: Prof. Dr. Jürgen Martens
Bei Industrieunternehmen anfallende Abfallstoffe werden als Edukte für die Synthese von neuen potentiellen Wirkstoffen und Reagenzien benutzt. Vorteil einer solchen Vorgehensweise : Abfallstoffe brauchen nicht verbrannt oder anderweitig entsorgt zu werden. Die Abfallstoffe stehen kostenfrei in ausreichenden Mengen zur Verfügung, der schmal bemessene Hochschuletat wird nicht durch den Kauf dieser Ausgangsstoffe belastet. Aus dem Abfallstoff wird eine Anzahl von potentiell brauchbaren Stoffen hergestellt. Ist die Forschung erfolgreich, so ist der Abfallstoff plötzlich ein begehrter Wertstoff.
Viele homochirale optisch aktive Wirkstoffe werden bis heute wirtschaftlich noch am ehesten durch eine Enantiomerentrennung aus dem Racemat hergestellt. Dabei fällt das ungewünschte Enantiomer in mindestens der gleichen Menge an, wie der homochirale optisch aktive Wirkstoff. Das unerwünschte Enantiomer kann in einigen Fällen racemisiert und anschließend recycliert werden. Doch das ist nicht in allen Fällen möglich. Hier setzen wir mit unseren Arbeiten an und suchen nach anderen Verwendungsmöglichkeiten für derartigen Abfall.
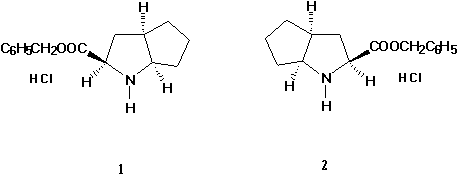
Konkret wurden z. B. von der Hoechst AG im letzten Jahr 20 kg (1R,3R,5R)-2-Azabicyclo[3.3.0]octan-3-carbonsäurebenzylester-Hydrochlorid 1 kostenlos zur Verfügung gestellt. In einem Schritt bei der Herstellung des Pharmawirkstoffes Ramipril der Hoechst AG findet eine Racematspaltung von (1RS,3RS,5RS)-2-Azabicyclo[3.3.0]octan-3-carbonsäurebenzylester statt. Für die Ramipril-Synthese benötigt man lediglich (1S,3S,5S)-2-Azabicyclo[3.3.0]octan-3-carbonsäurebenzylester-Hydrochlorid 2, die gleiche Menge des Abfallstoffs 1 fällt zwangsläufig an und muß entsorgt werden. Ziel der synthetischen Forschung ist die Suche nach nützlichen Verwendungsmöglichkeiten für 1, vor allem sollen neue Reagenzien und Katalysatoren für die asymmetrische Synthese gewonnen werden. Die ersten Resultate sind in Publikationen niedergelegt. Die Arbeiten werden fortgesetzt.
Bisher sind aus Hochschulen oder staatlichen Forschungsinstituten keine Arbeiten zur Verwertung des Abfallstoffs 1 bekannt geworden.

Bei der Hydroformylierung von Alkenen fallen erhebliche Mengen unerwünschter verzweigter Aldehyde als Abfallstoff an. Beim Wacker-Verfahren zur Erzeugung von Acetaldehyd aus Ethylen entsteht als Nebenprodukt zwangsläufig Chloracetaldehyd. Dies sind weitere Beispiele für zwangsweise anfallende Abfallstoffe, für die es keine ausreichende Verwendung gibt. Wir haben aus diesen Abfallstoffen eine Vielzahl neuer heterocyclischer Verbindungen, Aminosäuren und geschützter Peptide synthetisiert. D-Penicillamin und D,L-Cystein werden inzwischen sogar im technischen Maßstab aus Abfall-Aldehyden hergestellt. Auch hier laufen derzeit weitere Forschungsarbeiten mit dem Ziel neue stoffliche Verwertungsmöglichkeiten für verzweigte Aldehyde zu finden.
Auswahl bisher erschienener Publikationen:
J. Wilken, S. Wallbaum, W. Saak, D. Haase, S. Pohl, L. N. Patkar, A. N. Dixit, P. Chittari, S. Rajappa und J. Martens: Utilization of Industrial Waste Materials, 6: Utilization of Derivatives of the Bicyclic Proline Analogue (all-R)-Octahydro-cyclopenta[b]pyrrol-2-carboxylic Acid in the stereoselective Synthesis, Liebigs Ann. Chem. 1996, 927-934.
J. Eilers, J. Wilken und J. Martens: Synthesis of new Chiral 1,2-Diamines and d-Aminoalcohols and their Application in Catalytic Enantioselective C-C Bond Formations at an Elevated Temperature of up to 110oC, Tetrahedron : Asymmetry 7 (1996) 2343-2361.
J. Wilken und J. Martens: Enantioselective Catalytic Borane Reduction of Prochiral Ketones: Synthesis ans Application of New Rigid b-Amino Alcohols with a Cycloalkanol Subunit, Synth. Commun. 26 (1996) 4477-4485.
Stand: laufend
Fremdfinanzierung: Hoechst AG
Dissertationen:
Uwe Kramer, Synthese und Verwendung von 4-Aryl-3-thiazolidinen und 3-Alkenoyl-3-thiazolidinen sowie der analogen Sauerstoffverbindungen, Oldenburg, 1993.
Die zukünftig geplanten Arbeiten sollen vor allem zu neuen Reagenzien und Katalysatoren für die asymmetrische Synthese führen. Weiterhin sollen neue chirale Selektoren für die chromatographische Racemattrennung entwickelt werden.
Enantioselektive Katalyse und asymmetrische Synthese
Projektleitung: Prof. Dr. Jürgen Martens
Ausgehend von verschiedenen enantiomerenreinen Aminosäuren werden 1,2-Aminoalkohole synthetisiert. Diese Aminoalkohole und daraus hergestellte Derivate werden dann als chirale Auxiliare in der stereoselektiven Synthese erprobt. Weiterhin werden die stereochemisch einheitlichen 1,2-Aminoalkohole als Liganden in der enantioselektiven homogenen Katalyse erprobt. Auch die Verwendung chiraler Diole und Diamine wird untersucht. Dabei geht es u. a. um
(a) die enantioselektive Reduktion prochiraler Ketone.
(b) die enantioselektive Alkylierung von Aldehyden.
(c) die enantioselektive Protonierung von Enolaten.
(d) die enantioselektive Hydrophosphonylierung von Iminen.
In einem weiteren Teilprojekt geht es um die Reduktion chiraler Ketone unter Verwendung chiraler Katalysatoren. Hier wird untersucht, ob es zu einer gegenseitigen Verstärkung der intramolekularen und der intermolekularen (= Wirkung des Katalysators) Induktion von Stereoselektivität kommt. Weiterhin wird untersucht, ob mittels hochwirksamer Katalysatoren sogar die intramolekulare Induktion aus den Substrat (Keton) heraus überspielt werden kann.
Stand: laufend
Fremdfinanzierung: DFG, JenaPharm AG, Hermann-Schlosser-Stiftung, Degussa AG
Kooperationen:
Prof. Dr. Jaques Muzart, Université Reims / Frankreich
Prof. Dr. Sasai, University of Tokyo / Japan
Prof. Dr. Byung Tae Cho, Hallym University / Südkorea
Prof. Dr. Romero Brunet, Universidad Autonoma Madrid / Spanien
Prof. Dr. Silvian Jugé, Université Cergy Pontoise / Frankreich
Prof. Dr. Shibasaki, University of Tokyo / Japan
Dissertationen:
Thomas Mehler, Darstellung neuer Chiralica aus a-Aminosäuren sowie deren Anwendung in der stereoselektiven Synthese und homogenen Katalyse, Oldenburg 1995.
Christine Dauelsberg, Darstellung von chiralen 1-(Aminoalkyl)cyclopentanolen und deren Anwendung in der stereoselektiven Synthese unter besonderer Berücksichtigung der enantioselektiven Katalyse, Oldenburg, 1996.
Auswahl bisher erschienener Publikationen:
C. Thorey, J. Wilken, F. Hénin, J. Martens, T. Mehler, J. Muzart: Diastereoselective Synthesis of Vinylmorpholines by Palladium-Catalyzed Tandem Allylic Substitutions using Enantiopure Aminoalcohols as Bifunctional Nucleophiles, Tetrahedron Lett. 36 (1995) 5527-5530.
S. J. Aboulhoda, S. Létinois, J. Wilken, I. Reiners, F. Hénin, J. Martens und J. Muzart: Palladium-Mediated Enantioselective Formation of 2-Methyltetral-1-one from the Corresponding Allyl or Benzyl Enol Carbonate in the Presence of Enantiopure Aminoalcohols, Tetrahedron : Asymmetry 6 (1995) 1865-1868.
V. Peper, K. Stingl, H. Thümler, W. Saak, D. Haase, S. Pohl, S. Jugé und J. Martens: Utilization of Industrial Waste Materials, 5: Synthesis of New, Chiral1,3,2-Oxazaphospholidine-Borane Complexes ans Attempts to Apply Them in the Stereoselective Synthesis, Liebigs Ann. Chem. 1995, 2123-2131.
I. Reiners, J. Wilken und J. Martens: Intramolecular vs. Intermolecular Induction in the Diastereoselective Catalytic Reduction of Enantiomerically Pure Ketones with Borane in the presence of Cyclic b-Amino alcohols, Tetrahedron : Asymmetry 6 (1995) 3063-3070.
I. Reiners, J. Martens, S. Schwarz, H. Henkel: Intramolecular vs. Intermolecular Induction in the Diastereoselective Catalytic Reduction of 17-Oxo-Steroides, Tetrahedron : Asymmetry 7 (1996) 1763-1770.
V. Peper und J. Martens: New b-Amino Alcohols as Chiral Ligands for the Catalytic Enantioselective Reduction of Prochiral Ketones and the Nucleophilic Addition of Diethylzinc to Benzaldehyde, Chem. Ber. 129 (1996), 691-695.
J. Martens: Reduction of Imino Groups (C=N) in (G. Helmchen, R. W. Hoffmann, J. Mulzer, E. Schaumann) Houben-Weyl Stereoselective Synthesis, Workbench Edition E21 Volume 7, S. 4199-4238, Thieme Verlag Stuttgart, 1996.
V. Peper und J. Martens: New Chiral Oxazaphospholidine Oxides as Highly Efficient Catalysts in the Enantioselective Reduction of Ketones, Tetrahedron Lett. 37 (1996), 8351-8354.
H. Gröger, Y. Saida, S. Arai, J. Martens, H. Sasai und M. Shibasaki: First Catalytic Asymmetric Hydrophosphonylation of Cyclic Imines: Highly Efficient Enantioselective Approach to a 4-Thiazolidinylphosphonate via Chiral Titanium and Lanthanoid Catalysts, Tetrahedron Lett. 37 (1996), 9291-9292.
Außerdem ist ein auf dem Gebiet der enantioselektiven und diastereoselektiven Reduktion enantiomerenreiner Ketone aus der Gruppe der 17-Keto-Steroide im Jahre 1994 angemeldetes Patent inzwischen erteilt worden.
Chromatographische Enantiomerentrennung
Projektleitung: Prof. Dr. Jürgen Martens
Ziel der Arbeiten ist die Synthese neuer chiraler Selektoren für die dünnschichtchrmatographische Enentiomerentrennung. Die chiralen selektoren werden hinsichtlich ihrer Trennwirkung in der DC getestet und mit kommerziellen Produkten (Chiralplate, Chir; beide vom Leiter der arbeitsgruppe bei einer früheren Industrietätigkeit entwickelt) verglichen. Gute neue chirale Selektoren sind für Industrieunternehmen interessant.
Stand: laufend
Fremdfinanzierung: Alexander von Humbold-Stiftung, Degussa AG, Macherey + Nagel, Hermann-Schlosser-Stiftung
Chemie von N/O- und N/S-Heterocyclen mit einer reaktiven C=N-Doppelbindung
Projektleitung: Prof. Dr. Jürgen Martens
Ziel der Arbeiten ist die Synthese neuer N/O- und N/S-Heterocyclen und deren Derivatisierung. Bei der Herstellung von Derivaten der 3-Oxazoline, 3-Thiazoline uns entsprechender Sechsringverbindungen gilt ein besonderes Augenmerk der Gewinnung neuartiger Phosphorverbindungen, die strukturelle Ähnlichkeiten mit Phosphonoaminosäuren aufweisen.
Stand: laufend
Fremdfinanzierung: Hermann-Schlosser-Stiftung, Degussa AG
Kooperationen:
Prof. Dr. Wolfgang Beck / Universität München
Prof. Dr. Schmutzler / Technische Universität Braunschweig
PD Dr. Sabine Köpper / Universität Oldenburg
Dissertationen:
Mostafa Hatam, Synthesis Of Five And Six-membered 1,3-2H-Heterocyclic Imines And Their Related Potentially Biologically Active Compounds, Oldenburg 1996.
Ausgewählte Veröffentlichungen und Patente:
M. Hatam, D. Tehranfar und J. Martens: A novel and convenient route to phosphonooligopeptides derived from 1,3-oxazolines, 1,3-oxazines and 1,3-thiazolines, Synth. Commun. 25 (1995) 1677-1688.
H. Gröger, M. Hatam und J. Martens : Synthese totalgeschützter, nichtproteinogener a-Aminosäuren und Oligopeptide aus 2H-1,3-Oxazinen und 2H-1,3-Benzoxazinen via Ugi-Reaktion, Tetrahedron 51 (1995) 7173-7180.
M. Hatam und J. Martens: Phosphinic Acid Analogues of Thiaproline and the Related Heterocyclic Amino Acids, Synth. Commun. 25 (1995) 2553-2559.
M. Hatam, S. Köpper und J. Martens: The Diastereoselective Synthesis of Oxacephams from 1,3-2H-Oxazines, Heterocycles 43 (1996) 675-683.
H. Gröger und J. Martens: Synthese totalgeschützter Thioanaloga der 1,2,3,4-Tetrahydrochinolin-2-carbonsäure aus 2H-1,4-Benzothiazinen via Ugi-Reaktion, Sulfur Lett. 19 (1996) 197-206.
H. Gröger und J. Martens: Synthesis of New 4-Thiazolidinylphosphonates via Stereoselective Pudovik Reaction, Synth. Commun. 26 (1996) 1903-1911.
H. Gröger, J. Wilken, J. Martens, I. Neda, H. Thönnessen, V. Pinchuk, P. G. Jones und R. Schmutzler: Stereoselektive Pudovik-Reaktion von 5,6-Benzo-2H-1-methyl-3-(2'-chlormethyl)-2-oxo-1,3,2l4-diazaphosphorinan-4-on mit einem 3-Thiazolin und MPL-chromatographische Isolierung des Überschußdiastereomers : Z. Naturforsch. 51b (1996) 1305-1312.
M. Hatam, J. Goerlich, R. Schmutzler, H. Gröger und J. Martens: The Totally Protected Hydroxy Containing a-Amino Phosphinic Esters and a-Amino Phosphinoxides as well as their Carmamoyl Derivatives, Synth. Commun. 26 (1996) 3685-3698.
H. Gröger, M. Hatam, J. Kintscher und J. Martens: Synthesis of Glutathione Analogues, Peptide Nucleic Acids and Phosphoneoligopeptides from Heterocyclic Imines, Synth. Commun. 26 (1996) 3383-3394.
M. Hatam, S. Köpper und J. Martens: Synthesis of Homohydantoin-Thiazolidine Bicyclic Compounds, Heterocycles 43 (1996) 1653-1663.
I. Neda, T. Kaukorat, P. G. Jones, R. Schmutzler, H. Gröger und J. Martens: Chemistry of the 1,3,5-Triaza-2-phosphorin-4,6-diones, Part XI. Base-Catalyzed Addition Reactions of 2-Oxo-2-hydro-1,3,5-trimethyl-1,3,5-triaza-2l4-phosphorine-4,6-dione to the C=N Double Bond of 3-Thiazoline Heterocycles, Z. Naturforsch. 51b (1996) 1486-1493.
H. Gröger, Y. Saida, S. Arai, J. Martens, H. Sasai und M. Shibasaki: First Catalytic Asymmetric Hydrophosphonylation of Cyclic Imines: Highly Efficient Enantioselective Approach to a 4-Thiazolidinylphosphonate via Chiral Titanium and Lanthanoid Catalysts, Tetrahedron Lett. 37 (1996), 9291-9292.
Mitglieder der Arbeitsgruppe
Fritz Bangert Dipl. Chem. Reiner Menkens,
Dr. Ursula Biermann Dipl. Chem. Daniele Mesch
Dr. Gerald Francke Christine Ohmstede
Dipl. Chem. Michael Blumenstein Axel Ortgies
Dipl. Chem. Ahlke Hayen Dipl. Ing. Karl-Heinz Plate
Dipl. Chem. Markus Kellmann Dr. Christine Schwager
Dipl. Chem. Matthias Lemmler Dr. Kay Schwarzkopf
Dr. Ralf Mahler Dr. Ralf Woisch
Lehre
Vorlesungen im Grundstudium
- Grundlagen der Organischen Chemie
- Reaktionsmechanismen in der Organischen Chemie
- Spektroskopische Methoden in der Organischen Chemie
Vorlesungen im Hauptstudium
- Reaktionsmechanismen in der Organischen Chemie für Fortgeschrittene (Physikalische Organische Chemie)
- Massenspektrometrie für Fortgeschrittene
- Präparative Radikalchemie
- Umweltverträgliche Organische Synthesen
Die Arbeitsgruppe ist an den Grund- und Fortgeschrittenenpraktika Organische Chemie beteiligt. In den Fortgeschrittenen Praktika werden u.a. Aufgaben bearbeitet, die den unten beschriebenen Forschungsgebieten entstammen. Intensiverer Einblick in die Forschungs- und Arbeitsgebiete ist im Rahmen eines freiwilligen Vertiefungspraktikums (ca. 6 Wochen) möglich.
Forschung
Die Arbeitsgruppe beschäftigt sich in der Forschung mit hochaktuellen Themen der organischen Chemie, die - inhaltlich eng miteinander verbunden - sowohl synthetische, reaktionsmechanistische als auch analytische Probleme sowohl der Grundlagenforschung als auch der angewandten Forschung umfassen.
Massenspektrometrische Untersuchungen
Unter wissenschaftlicher Mitarbeit von: Dr. Ralf Woisch, Dr. Christine Schwager, Dipl. Chem. Markus Kellmann, Dipl. Chem. Reiner Menkens
- Die eindeutige und schnelle Charakterisierung von Biopolymeren ist von allergrößtem wissenschaftlichen und auch praktischen Interesse. Wir untersuchen mit neuen massenspektrometrischen Methoden wie der Matrixunterstützten Laserdesorptionsionisations-Massenspektrometrie (MALDI-MS) Biopolymere - insbesondere Polysaccharide und Lignine - mit dem Ziel, diese Makromoleküle unzerstört nachzuweisen, Strukturinformationen zu erhalten und ihr Molekulargewicht und die Molekulargewichtsverteilung zu bestimmen.
- Der Nachweis und die Charakterisierung reaktiver Zwischenstufen bei komplexen Reaktionen in Lösung ist von größter Bedeutung für die Aufklärung von Reaktionsmechanismen und damit für das Verständnis und die Lenkung chemischer Reaktionen. Neuentwickelte massenspektrometrische Ionisierungsmethoden wie die chemische Ionisation bei Atmosphärendruck (APCI) und Elektrospray-Ionisation (ESI) erlauben die direkte massenspektrometrische Untersuchung von Lösungen. Die hohe Empfindlichkeit und der große dynamische Bereich der Massenspektrometrie machen diese Methoden zu einem idealen Werkzeug zur Untersuchung von Reaktionen in Lösung und zum Nachweis der nur in sehr kleinen Konzentrationen vorkommenden reaktiven Zwischenstufen. Ziel der Forschungsarbeit ist es, eine neue Methode zur Untersuchung von Reaktionen in Lösung und zum Nachweis der dabei auftretenden reaktiven Zwischenstufen mit Hilfe der APCI- und ESI-Massenspektrometrie zu entwickeln. Im Mittelpunkt stehen die neutralen Spezies und hier insbesondere die Radikale.
Fremdfinanzierung: DFG
Kooperation mit: Institut für Holzchemie der Bundesforschungsanstalt für Holzforschung, Hamburg / Prof. Dr. O. Faix, Dr. J. Puls; Fachbereich Physik, Universität Oldenburg / Dr. W. Tuscynski, Prof. Dr. E. Hilf
Dissertation: Christine Schwager, Isolierung von Lignin-Kohlenhydrat-Komplexen und ihre Charakterisierung durch enzymatischen Abbau sowie Matrixunterstützte Laserdesorptions-Massenspektrometrie, Oldenburg und Hamburg 1996.
Diplomarbeit: Markus Kellmann, Massenspektrometrische Untersuchungen an Radikalen, 1996
Tagungsbeiträge
Jürgen O. Metzger, R. Woisch, C. Schwager, R. Angermann, O. Faix und W. Tuscynski, Matrix-unterstützte Laserdesorptions-Massenspektrometrie von Ligninen, AGMS, Tübingen, 6.-9.6.1995.
Jürgen O. Metzger, R. Woisch, C. Schwager, O. Faix, Massenspektrometrische Untersuchungen von Ligninen, AGMS, Tübingen, 6.-9.6.1995
C. Schwager, O. Faix, J. Puls and J.O. Metzger, Characterization of Lignin-Carbohydrate Complexes by DDQ Oxidation, Abstracts of Papers of the American Chemical Society, 1996, 211, 52.
Öle und Fette als nachwachsende Rohstoffe für die Chemie - Umweltverträgliche organische Synthesen
Unter wissenschaftlicher Mitarbeit von: Dr. Ursula Biermann, Dr. Manfred Bischoff, Dr. Gerald Francke, Axel Ortgies, Daniele Mesch
- Radikalische und Lewis Säure induzierte Additionen an ungesättigte Fettstoffe: Bereitstellung neuartiger Fettstoffe
Im Rahmen eines umfangreichen Projekts wird die chemische Nutzung von Pflanzenölen als nachwachsende Rohstoffe untersucht. Ölsäure, Erucasäure, Petroselinsäure und andere Fettsäuren, die in relativ großer Reinheit aus Pflanzenölen zu gewinnen sind, und die entsprechenden nativen Öle werden unter Nutzung der modernen Synthesemöglichkeiten insbesondere durch Reaktionen an der Doppelbindung vielfältig modifiziert. Damit werden die physikalischen Eigenschaften verändert und möglicherweise neue Anwendungsmöglichkeiten für Fettstoffe erschlossen. Die neuartigen Fettstoffe werden in zahlreichen Betrieben der chemischen Industrie auf ihr Anwendungspotential als Bausteine für Kunststoffe, als Schmier- und Gleitmittel, als oberflächenaktive Verbindungen, als Wirkstoffe im Pflanzenschutz und für weitere Zwecke untersucht. Ein weiterer Gesichtspunkt dieser Arbeiten ist die Entwicklung von Methoden für neue umweltverträgliche Synthesen.
Fremdfinanzierung: Bundesministerium für Ernährung, Landwirtschaft und Forsten
Kooperation mit: Prof. Warwel, Bundesanstalt für Getreide-, Kartoffel- und Fettforschung, Münster / Dr. Lang, TU Braunschweig / Prof. Schäfer, Universität Münster / Prof. Schneider, GHS Wuppertal / Fa. Bayer, Leverkusen / Fa. Henkel, Düsseldorf / Fa. Hoechst, Frankfurt / Fa. BASF, Ludwigshafen.
- Neue Wege zur Synthese linearer primärer Alkohole und chlorfreier Alkyltetrahydropyranderivate. Umsetzung von Ergebnissen aus der Hochschulforschung in die Industrielle Praxis.
Fremdfinanzierung: Stiftung Industrieforschung
Kooperation mit: Condea Chemie GmbH, Brunsbüttel
- Einsatzmöglichkeiten derivatisierter nativer Öle und Fette als Chemierohstoffe in der kautschukverarbeitenden Industrie.
Fremdfinanzierung: Stiftung Industrieforschung
Kooperation mit: Schill und Seilacher, Hamburg
Die Arbeitsgruppe war 1995 am Gemeinschaftsstand der niedersächsischen Hochschulen auf der Hannover Messe beteiligt.
Diplomarbeit: Daniele Mesch, Umweltfreundliche organische Synthesen - Kriterien und Beispiele, 1995.
Veröffentlichungen
J.O. Metzger and Fritz Bangert, Ane Additions to Unsaturated Fatty Compounds: Thermally Initiated Additions of Alkanes to Methyl 10-Undecenoate, Fat Sci. Technol. 1995, 97, 7-9.
J.O. Metzger und R. Mahler, Lösungsmittelfreie, durch Elektronenübertragung von Kupfer initiierte radikalische Additionen von aktivierten Halogenalkanen an Alkene, Angew. Chem. 1995, 107, 1012-1015; Angew. Chem. Int. Ed. Engl. 1995, 34, 902-904.
J.O. Metzger and U. Biermann, Ethylaluminium Dichloride Induced Reactions of Acetals with Unsaturated Carboxylic Esters: Synthesis of Homoallyl Ethers, Liebigs Ann. 1996, 1851-1854.
J.O. Metzger, R. Mahler and A. Schmidt, Electron Transfer Initiated Free Radical Additions of Perfluoroalkyl Iodides and Diiodides to Alkenes, Liebigs Ann. 1996, 693-696.
J.O. Metzger, U. Biermann und R. Mahler, Neuartige funktionalisierte und verzweigte Fettstoffe, in „Perspektiven nachwachsender Rohstoffe in der Chemie" (Hrsg. H. Eierdanz), 1996, VCH Weinheim, S. 255.
U. Biermann and J.O. Metzger, Lewis Acid Induced Additions to Unsaturated Fatty Compounds, in Oils-Fats-Lipids, Proceedings of the 21st World Congress of the International Society for Fat Research (ISF), Den Haag 1995 (Ed. PJ Barnes & Associates), Thamesluik Ltd, Windsor 1996, Vol. 3, S. 457-459.
J.O. Metzger, U. Linker and R. Mahler, Electron Transfer Initiated Free Radical Additions to Unsaturated Fatty Compounds, in Oils-Fats-Lipids, Proceedings of the 21 st World Congress of the International Society for Fat Researcz (ISF), Den Haag 1995 (Ed. PJ Barnes & Associates), Thamesluik Ltd., Windsor 1996, Vol. 3, S. 477-479.
Tagungsbeiträge:
Jürgen O. Metzger und Ralf Mahler, „Umweltverträgliche organische Synthesen: Lösungsmittelfreie, durch Elektronenübertragung von Kupfer initiierte radikalische Additionen von aktivierten Halogenalkanen an Alkene, GDCh-Hauptversammlung, 10.-16.9.1995, Münster.
Ralf Mahler und Jürgen O. Metzger, Elektronentransfer initiierte radikalische Additionen an ungesättigte Fettstoffe, GDCh-Hauptversammlung, 10.-16.9.1995, Münster.
Ursula Biermann und Jürgen O. Metzger, „Lewis Säure induzierte C,C-Verknüpfungen an ungesättigten Fettstoffen", GDCh-Hauptversammlung, 10.-16.9.1995, Münster
Ursula Biermann und Jürgen O. Metzger, „Synthese neuartiger Fettstoffe : Ionische Additionen an ungesättigte Fettstoffe", 1. Jahrestagung des BML-Forschungsverbunds „Chemische Nutzung heimischer Pflanzenöle", 9.10.1995, Braunschweig.
Jürgen O. Metzger, Ralf Mahler, Gerald Francke und Ursula Biermann, „Bereitstellung neuartiger Fettstoffe", 1. Jahrestagung des BML-Forschungsverbunds „Chemische Nutzung heimischer Pflanzenöle", 9.10.1995, Braunschweig.
Jürgen O. Metzger und Ursula Biermann, „Synthese von Fettstoffen mit Homoallyletherfunktion", 51. DGF-Jahrestagung, 6.-8.10.1996, Bremen.
Gerald Francke und Jürgen O. Metzger, „Synthese von neuartigen Fettstoffen mit Amidfunktionen", 51. DGF-Jahrestagung, 6.-8.10.1996, Bremen.
Manfred Bischoff und Jürgen O. Metzger, „Synthese neuartiger heterocyclischer Fettstoffe", 51. DGF-Jahrestagung, 6.-8.10.1996, Bremen.
Selektivität radikalischer Reaktionen
Unter wissenschaftlicher Mitarbeit von: Dipl. Chem. Michael Blumenstein, Dr. Gerald Francke, Dipl. Chem. Ahlke Hayen, Dipl. Chem. Matthias Lemmler, Dr. Kay Schwarzkopf
Die Selektivität chemischer Reaktionen ist ein grundlegendes Problem der Chemie und von überragender praktischer Bedeutung. Untersucht werden die Selektivität radikalischer Elementarreaktionen wie Addition, Fragmentierung und Wasserstoffabstraktion. Ziel der Untersuchungen ist, einen genaueren Einblick in den Übergangszustand chemischer Reaktionen zu gewinnen, den Mechanismus komplexer Reaktionen aufzuklären und damit für die präparative Chemie Daten zur optimalen Reaktionsführung bereitzustellen. Von größtem aktuellen Interesse ist die Untersuchung der Stereoselektivität und insbesondere der Enantioselektivität intermolekularer radikalischer Reaktionen und der Einsatz radikalischer Reaktionen in der Synthese.
Fremdfinanzierung: DFG
Kooperation mit: Ben-Gurion University of the Negev, Beer Sheva / Dan Meyerstein
Dissertationen:
Gerald Francke, Zur Diastereoselektivität der radikalischen Wasserstoffübertragung auf acyclische Trifluormethylalkyl-Radikale, Universität Oldenburg, 1995.
Kay Schwarzkopf, Enantioselektivität der radikalischen Wasserstoffübertragung auf acyclische prochirale Radikale, Universität Oldenburg, 1996.
Diplomarbeiten:
Ahlke Hayen, Synthese eines chiralen Zinnhydrids und sein Einsatz in der enantioselektiven Reduktion von prochiralen Alkylradikalen, Universität Oldenburg, 1996.
Matthias Lemmler, Synthese und Racematspaltung von substituierten Aminoindanderivaten, Universität Oldenburg, 1997
Veröffentlichungen:
M. Blumenstein, K. Schwarzkopf und J.O. Metzger, Enantioselektive Wasserstoffübertragung von einem chiralen Zinnhydrid auf ein prochirales kohlenstoffzentriertes Radikal, Angew. Chem. 1997, 107, 245-247; Angew. Chem. Int. Ed. Engl. 1997, 107, 235-236.
K. Schwarzkopf, J.O. Metzger, W. Saak and S. Pohl, Synthesis of Novel Optical Active Tin Hydrides Containing Chiral Ligands, Chem. Ber. 1997, to be published.
Tagungsbeiträge:
K. Schwarzkopf and J.O. Metzger, Enantioselective Transfer of Hydrogen Atoms to Acyclic Prochiral Alkyl Radicals, Gordon Research Conference on Free Radical Reactions, 24.7. - 28.7.1995.
Jürgen O. Metzger, Kay Schwarzkopf und Michael Blumenstein, Untersuchungen zur Enantioselektivität der radikalischen Wasserstoffübertragung, GDCh-Hauptversammlung, 10.-16.9.1995, Münster.
Jürgen O. Metzger, Michael Blumenstein, Ahlke Hayen and Kay Schwarzkopf, Enantioselective Transfer of Hydrogen Atoms to Prochiral Alkyl Radicals Using Chiral Hydrogen Donors, The Seventh International Symposium on Organic Free Radicals, June 16-21, 1996, Bardolino, Italien.